商机详情 -
南昌外泌体提取试剂厂家现货
由欧洲多国细胞外囊泡领域的学者发起并成立的国际细胞外囊泡协会(ISEV)于2014年在协会会刊JournalofExtracellularVesicles发表了一个指导性意见,也就是我们常说的MISEV2014。2018版《指导要求》进行了修订。2018版的《指导要求》首先讨论了对这些细胞来源的非细胞具膜结构如何称呼。学者们普遍认为应当使用细胞外囊泡(extracellularvesicle)来称呼这些具膜囊泡,当我们使用常规方法分离这些结构时不推荐使用其他的名称来称呼它们。使用PBS对膜进行洗脱即得到外泌体浓缩液。南昌外泌体提取试剂厂家现货

人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。三是外泌体膜可以与靶细胞膜直接融合,非选择性的释放其所含的蛋白质、mRNA以及microRNA南昌外泌体提取试剂厂家现货外泌体的提取方法:密度梯度离心。
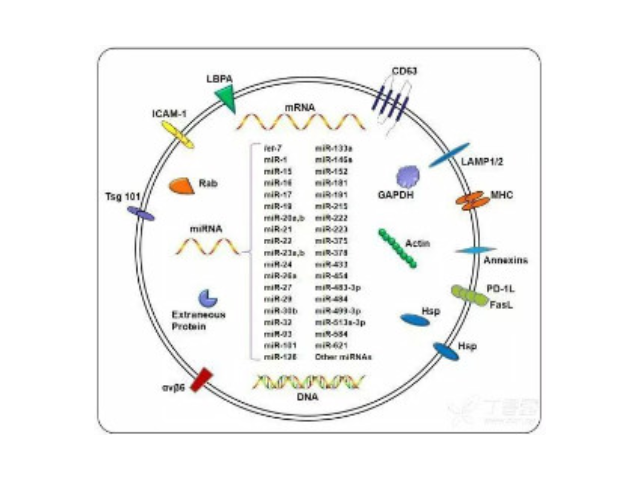
1983年,外泌体初次于绵羊网织红细胞中被发现,1987年Johnstone将其命名为“exosome”。多种细胞在正常及病理状态下均可分泌外泌体。其主要来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。所有培养的细胞类型均可分泌外泌体,且外泌体天然存在于体液中,包括血液、唾液、尿液、脑脊液和乳汁中。有关他们分泌和摄取及其组成、“运载物”和相应功能的精确分子机制刚刚开始研究。外泌体目前被视为特异性分泌的膜泡,参与细胞间通讯,对外泌体的研究兴趣日益增长,无论是研究其功能还是了解如何将其用于微创诊断的开发。如何高效地提取外泌体是实现这项新兴液体活检技术临床常规化应用的关键。
作为一种分子通断开关的KRAS发生突变时会处于“开启”状态。在80%~95%的胰腺导管腺病(PDAC)当中,这个基因发生突变,这也是这种一些疾病中较为常见的突变。这些研究人员证实iExosome能够运送特异性地靶向KRAS的siRNA和shRNA分子,并且比他们的合成对应物脂质体(liposome)更加高效。脂质体不具有外泌体表现出的天然复杂性和优势。德州大学MD安德森一些疾病中心一些疾病生物学助理教授ValerieLeBleu博士说,“我们的研究提示着与脂质体相比,外泌体表现出运送siRNA分子和压制侵袭性胰腺瘤生长的优异能力。我们也证实外泌体表面上的CD47存在允许它们躲避来自循环单核细胞的吞噬作用。”外泌体提取:尺寸排阻色谱可以精确分离大小分子。

有的外泌体分离方法需要高速离心,需要使用大型机器,耗费近24小时的时间才能获得,非常不便。而高离心力也可能破坏囊泡。降低样品的质量。这项研究有望解决这一难题。在论文中,研究人员们提供了一种通过微流体和声学的独特组合从体液样品中捕获外泌体的新颖方法。他们开发的原始声学分选装置由两个倾斜的声学换能器和一个微流体通道组成,当这些传感器产生的声波相互碰撞时,形成产生一系列压力节点的驻波。每当细胞或颗粒流过通道并遇到一个节点时,压力会将细胞引导离开中心一点点。细胞移动的距离取决于大小和其他属性(如可压缩性),这样,当到达通道末尾时,不同大小和性质的细胞就能够被分离开来。这种方法分离得到的外泌体,基本上不改变其生物或物理特征,为开发评估人类健康以及疾病诊断和进展提供了有吸引力的新方法。用于外泌体提取的体液收集注意事项:选择血清还是血浆?推荐大多数研究选择血浆。南昌外泌体提取试剂厂家现货
由于国内有关外泌体提取试剂的缺乏,我国对外泌体的研究还基本依赖于过程繁琐的超速离心和进口提取试剂盒。南昌外泌体提取试剂厂家现货
外泌体的提取、分离方法:免疫亲和层析法。免疫亲和层析法是利用生物体内存在的抗原、抗体之间高度特异性的亲和力进行分离的方法,主要用于生物大分子的分离、纯化。将其应用于外泌体的分离主要是借助外泌体表面的特异性抗体,如TSG101或四跨膜蛋白。此方法的原理是利用抗原抗体的特异性结合,只有囊泡表面有特异性的抗体才可以被识别,这使得提取的外泌体纯度高,但是产量低。Zarovni等分别用超速离心、密度梯度离心和免疫层析法,从血浆和细胞上清中提取外泌体蛋白,结果表明,免疫亲和层析法得到的外泌体表面存在多种标记蛋白(Alix、CD9、CD63),同时,ELISA和PCR结果也证明了该方法的可行性。南昌外泌体提取试剂厂家现货